|
|
|
#1
|
|||
|
|||
|
عند الاطلاع علي شرح خلية الوقود في كتاب المدرسة وجدت انا الشرح غير متوافق مع الرسم المرافق
فذكر ان الالكتروليت هو هيدروكسيد البوتاسيوم (لابد ان تكون الايونات المتواجدة هي الهيدروكسيد oh-) نجد الايونات في الرسم هي الهيدروجين الموجب وفي المعادلات الماء يتكون عند الانود في الرسم متكونة عند الكاثود الخلاصة ان الرسمه لنوع اخر من خلايا الوقود وهي الحامضية التي يستخدم حمض الفوسفوريك كالتروليت فيكون الالتروليت يحتوي علي ايونات الهيدروجين الموجب والماء يتكون عند الكاثود |
|
#2
|
|||
|
|||
|
اقتباس:
__________________
محمد عبد السلام عواد كتاب الوافي في الكيمياء |
|
#3
|
|||
|
|||
|
اسمح لي استاذي الفاضل ان اختلف مع حضرتك لات الرسم الموجود بكتاب المدرسة هو لخلية الوقود الحمضية والتي يحتوي الالكتروليت (حمض الفوسفورك) علي ايةنات الهيدروجين الموجبة ويكون التفاعلات كالاتي تفاعل الانود : 2h2=4h+4e تفاعل الكاثود : o2+4h+4e=2h2o اي ان الماء تكون عند الكاثود ومن البديهي عندما يكون الالكتروليت قلوي يكون ايونات الهيدروكسيد هي السائدة وحتي لو وصل اليها ايونات هيدروجين فانها تتحد مع جزء من هذه الايونات وتكون ماء ولا توجد في هذه الحالة ايونات هيدروجين موجبة حرة ولكن الذي يظهر هو الهيدروكسيد السالب والشكر الجزيل لسيادتكم
|
|
#4
|
|||
|
|||
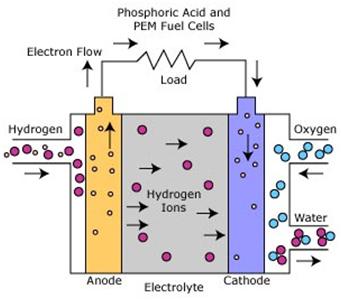 خلايا الوقود الحمضية الفسفورية من أول أنواع الخلايا التي توفرت بشكل تجاري. بدأ تطويرها منذ منتصف الستينات وبدأت التجارب عليها بالسبعينات,لذا فهي متطورة من ناحية أداءها واستقرارها وكلفتها.هذه الخصائص جعلت من الخلايا الحمضية الفسفورية مرشحاً جيداً للاستخدام مبكراً. تستخدم خلايا الوقود (PAFC) الحمض الفسفوري (phosphoric acid (H3PO4)) كوسيط حيث أن التشرد لهذا الوسيط هو 100%.لكن نسبة التشرد هذه تنخفض مع انخفاض درجة الحرارة لذا فخلايا الحمض الفسفوري تحتاج لحرارة عالية للعمل بحدود (150ºC-220ºC) . حاملات الشحنة في هذا النوع من خلايا الوقود هي ايونات الهيدروجين (H+, proton). كما في خلايا الوقود ذات غشاء التبادل البروتونات (PEMFC) حيث يتم توصيل الهيدروجين إلى القطب الموجب anode ويتم فصله لبروتون والكترون. تمر البروتونات خلال الوسيط وتندمج مع الأكسجين (غالبا من الهواء )في القطب السالب cathode لتكون الماء. الالكترونات السالبة تتحرك في دارة كهربائية خارجية بحيث نحصل على كهرباء وعمل مفيد. هذه العمليات الجارية في خلية الوقود تنتج كهرباء وحرارة . التفاعلات في القطب الموجب (Anode Reaction) 2 H2 ⇒ 4 H+ + 4 e- التفاعلات في القطب السالب (Cathode Reaction) O2(gas) + 4 H+ + 4 e- ⇒ 2 H2O التفاعل النهائي (Overall Cell Reaction) 2 H2 + O2 ⇒ 2 H2O آخر تعديل بواسطة سيد عثمان ، 02-02-2016 الساعة 11:53 AM |
|
#5
|
|||
|
|||
|
اقتباس:
---------------------------------------------------------------------------------------------- فعلا كان المفروض الصورة دي ---------------------------------------------------------------------------------------------- 
آخر تعديل بواسطة meshfaker ، 12-02-2016 الساعة 03:56 PM سبب آخر: ليكون اوضح |
|
#6
|
||||
|
||||
|
فعلا الرسمة اللى فى كتاب المدرسة مش مطابقة للشرح ورسمتها مختلفة تماما بس هنعمل اي ..لازم نحطها كده فى الامتحان ..الى ان يشاء الله وتتعدل
__________________
هون عليك فإن الله فارجها فربك وحده يدري كيف مخرجها 💟🌷 |
|
#7
|
|||
|
|||
|
بجد ربنا يبارك لكم تعبكم وتكونوا دايما عونا لنا ونتعلم منكم
|
|
#8
|
||||
|
||||
|
خلايا الوقود انواعها متعددة وكثيرة والنوع الموجود بكتاب الوزارة يتم فيه استخدام اكسيجين الهواء الجوى مع الهيدروجين النقي ونلاحظ دخول بخار ماء مع الاكسيجينفي رسم كتاب الوزارة اما خلايا سفن الفضاء فيستخدم الاكسيجين النقى مع الهيدروجين النقي
__________________
 مستر// فيكتور بخيت مستر// فيكتور بخيتاستاذ الكيمياء |
|
#9
|
|||
|
|||
|
الجزء الخطأ في رسمة الكتاب الالكتروليت ومكان خروج الماء
|
|
#10
|
|||
|
|||
|
اخى ميمو البطل الالكتروليت سليم مفيش مشكله فيه
ولفهم كيفية حدوث التفاعلات الحادثه داخل الخليه يبقى كالاتى الحجره الوسطيه بها محلول هيدروكسيد البوتاسيوم وهو الكتروليت قوى تام التاين يعنى الحجره الوسطيه بها ايونات بوتاسيوم موجب وايونات هيدروكسيل سالبه بالاضافه الى ماء المحلول ----------------------------------------------------------------------------- عند دفع تيار غاز الهيدوجين فان الكربون المسامى يعمل على ادمصاص الغاز وعند دخول غاز الهيدروجين الى حجرة الانود عبر الكربون المسامى فانه يتاين فى حجرة الانود مكونا ايونات الهيدروجين والالكترونات التى تندفع عبر سلك خارجى حتى تصل الى حجرة الكاثود اما ايونات الهيدروجين الموجبه فتنتقل عبر الكربون المسامى الى الحجره الوسطيه فيزداد تركيز ايونات الهيدروجين الموجبه تدريجيا فى الحجره الوسطيه على حساب تركيز ايونات الهيدروكسيل السالبه بتاعت هيدروكسيد البوتاسيوم اى تقل الصفه القلويه تدريجيا فى الحجره الوسطيه فيزيادة تركيز ايونات الهيدروجين الموجبه فى الحجرة الوسطيه ------------------------ ---------------------------------------------------------------- عندما يدفع تيار الاكسجين من فتحه جانبيه فان الكربون المسامى يدمصه فيدخل فى حجرة الكاثود فيكتسب الالكترونات القادمه من حجرة الانود بالاضافه الى الماء الموجود فى محلول هيدروكسيد البوتاسيوم فيختزل الى مجموعات هيدروكسيل فى الحجرة الوسطيه فيزداد تركيز ايونات الهيدروكسيل تدريجيا ليقاوم الزياده فى تركيز ايون الهيدروجين الموجب فتتحد ايونات الهيدروجين الموجب فى الحجره الوسطيه مع ايونات الهيدروكسيل الناتجه من التفاعلات مكونه الماء الذى يخرج من فتحه جانبيه فيظل تركيز هيدروكسيد البوتاسيوم ثابت فى الحجره الوسطيه اثناء عمل الخليه اى يعود هيدروكسيد البوتاسيوم لتركيزه الاصلى مره اخرى ارجو ان تكون وصلت هناك ابحاث لانتاج خلايا وقود يستخدم فيها غاز الميثان ووقود الديزل لانتاج الطاقه الكهربيه مباشرة دون الحاجه لانتاج غاز الهيدروجين اولا من هذه المواد مستر /عبد الناصر صديق محمود آخر تعديل بواسطة عبدالناصر صديق ، 29-02-2016 الساعة 02:26 AM سبب آخر: خطا كتابى |
|
#11
|
||||
|
||||
 تعتبر خلية الوقود أداة لتحويل الطاقة الكيميائية إلى طاقة كهربية اي انها تقوم من خلال تفاعلات كيميائية بتحويل الهيدروجين والاكسجين إلى ماء وينتج عن هذه العملية طاقة كهربية. وبالمقارنة مع البطارية التقليدية المعروفة فإن الاختلاف يكمن في ان المواد الكيميائية الداخلة في التفاعل لتوليد الكهرباء هي جزء من تركيب البطارية وتوجد في داخلها، وبانتهاء المواد الكيميائية هذه فإن البطارية تصبح عديمة الفائدة ويتم استبداله أو اعادة شحنها مرة اخرى، في حين ان خلايا الوقود لا يمكن ان تنتهي فهي تعمل باستمرار لان مصدر المواد الكيميائية هي من الهواء.  شرائح من خلايا الوقود تستخدم كمصدر للطاقة في السيارات يوجد العديد من خلايا الوقود تصنف حسب المواد الكيميائية التي تستخدمها، وكذلك صفائح المحلل electrolyte التي تستخدماها. والنوع الاكثر شيوعا ورواجا هو خلية الوقود ذات غشاء التبادل البروتوني proton exchange membrane fuel cell (PEMFC) والموضح فكرة عملها في الشكل التالي:  فكرة عمل وتركيب خلية الوقود لانتاج الطاقة الكهربية يوضح الشكل اعلاه تركيب خلية الوقود وفكرة عملها تتلخص في المراحل التالية:  هذه هي التفاعلات الكيميائية التي تحدث على طرفي الخلية  إن النماذج البسيطة التي تصنع منها الخلية الهيدروجينية والمستخدمة في وسائط النقل تنتج والي 1.16 Volt لذلك يتم وصل عدد كبير من الخلايا لتوليد الطاقة الكهربائية المطلوبة . يبين الشكل التالي خلية هيدروجينية مكونة من عدد كبير من الشرائح لتوليد فرق الجهد المطلوب.  لقد تنوعت أماكن استخدام الخلية الهيدروجينية واختلفت التصاميم و الأبعاد الموضوعة لها تبعاً للطاقة المطلوبة منها وفي الصورتين التاليتن مثالاً لذلك  دراجة نارية تستخدم وقود الهيدروجين بدلا من الوقود التقليدي من خلال خلايا الوقود  سيارة تعمل بواسطة محرك كهربي يحصل على الطاقة من خلايا الوقود الهيدروجيني    
__________________
( الاستاذ محمد الطنطاوى) استاذ الكيمياء بمدرسة فيشا سليم الثانوية المشتركة |
|
#12
|
||||
|
||||
|
فيديو ممتاز لخلية الوقود
https://www.youtube.com/watch?v=FnldcmTIdbM
__________________
( الاستاذ محمد الطنطاوى) استاذ الكيمياء بمدرسة فيشا سليم الثانوية المشتركة |
 |
| العلامات المرجعية |
«
الموضوع السابق
|
الموضوع التالي
»
| أدوات الموضوع | |
| انواع عرض الموضوع | |
|
|
جميع الأوقات بتوقيت GMT +2. الساعة الآن 11:47 PM.












 العرض المتطور
العرض المتطور
